Archives pour la catégorie Non classé
Navigation des articles
Guide du parcours de soins – Patients présentant une suspicion de borréliose de Lyme
Guide du parcours de soins – Patients présentant une suspicion de borréliose de Lyme – HAS mars 2022
Prise en charge en soins primaires
Prise en charge en centre de compétences des MVT (CC MVT)
Prise en charge en centre de références des MVT (CR MVT)
mars 2022
mars 2022
dispositif VIH Test : sérologie VIH sans ordonnance
Depuis le 1er janvier 2022, le dispositif VIH Test est effectif sur tout le territoire national. Ainsi, toute personne peut désormais demander un dépistage du VIH en laboratoire sans prescription et sans avance de frais.
Sauf personnes non éligibles: les patients majeurs sans droit ouvert, les souhaits d anonymat, les patients mineurs.
Ils peuvent s’orienter vers un Centre Gratuit d’information, de Dépistage et de Diagnostic (CeGIDD) (acte gratuit et anonyme) (voir sur https://www.sida-info-service.org/annuaire ou 0 800 840 800)
Sauf personnes non éligibles: les patients majeurs sans droit ouvert, les souhaits d anonymat, les patients mineurs.
Ils peuvent s’orienter vers un Centre Gratuit d’information, de Dépistage et de Diagnostic (CeGIDD) (acte gratuit et anonyme) (voir sur https://www.sida-info-service.org/annuaire ou 0 800 840 800)
Ouvertures des laboratoires de biologie médicale dans la région le week-end de Paques
concernant les demandes de PCR pour des bilans pre-opératoire ou pour des départs en avion le mardi, vous trouverez dans le lien suivant les sites de LBM ouverts le dimanche et lundi de Paques:
URPS Biologistes Occitanie – Actualités COVID-19 (urps-biologistes-occitanie.fr)
URPS Biologistes Occitanie – Actualités COVID-19 (urps-biologistes-occitanie.fr)
VILLEFRANCHE DE ROUERGUE – RENDEZ-VOUS
A COMPTER DU 10/01/2022
TOUS LES PRELEVEMENTS (Y COMPRIS LES COVID) SERONT EXCLUSIVEMENT SUR RDV SUR LE SITE www.doctolib.fr
TOUS LES PRELEVEMENTS (Y COMPRIS LES COVID) SERONT EXCLUSIVEMENT SUR RDV SUR LE SITE www.doctolib.fr
Tests de dépistage RT-PCR COVID-19 (nasopharyngés et salivaires)
A partir du 15 octobre 2021, les tests de dépistage RT-PCR COVID-19 (nasopharyngés et salivaires) ne seront plus systématiquement pris en charge par l’assurance maladie sauf exceptions.
Les exceptions sont : les mineurs, les personnes munies d’une prescription médicale de moins de 48 heures (sauf opération programmé : date d’intervention à mentionner sur l’ordonnace), les personnes vaccinées si symptomatique, les élèves du secondaire de plus de 18 ans, les personnes contacts identifiées par la CPAM.
Ces tests seront facturés 43,90 € si le prélèvement est réalisé au laboratoire ou 34,30 € si le prélèvement est réalisé en dehors du laboratoire.
Les cas de prise en charge par l’assurance maladie sont détaillés dans le tableau ci-dessous ainsi que les pièces justificatives à fournir.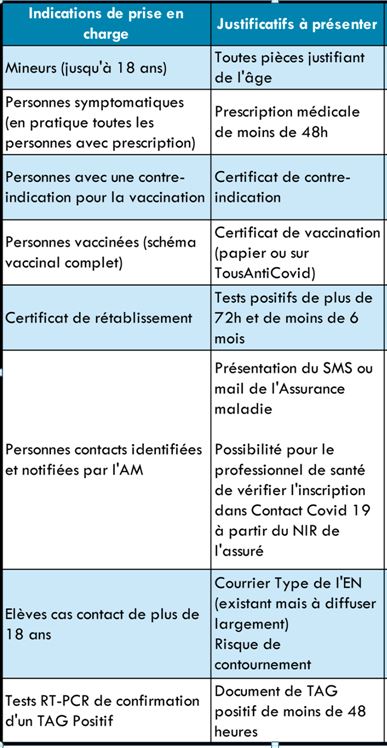
octobre 2021
Les exceptions sont : les mineurs, les personnes munies d’une prescription médicale de moins de 48 heures (sauf opération programmé : date d’intervention à mentionner sur l’ordonnace), les personnes vaccinées si symptomatique, les élèves du secondaire de plus de 18 ans, les personnes contacts identifiées par la CPAM.
Ces tests seront facturés 43,90 € si le prélèvement est réalisé au laboratoire ou 34,30 € si le prélèvement est réalisé en dehors du laboratoire.
Les cas de prise en charge par l’assurance maladie sont détaillés dans le tableau ci-dessous ainsi que les pièces justificatives à fournir.

octobre 2021
Carte de groupe
Les cartes de groupe sanguin ne sont plus éditées systématiquement et ne le seront que sur demande expresse du patient lors de la remise de résultats au laboratoire
PASS SANITAIRE
FAQ PASS SANITAIRE
https://www.gouvernement.fr/pass-sanitaire-toutes-les-reponses-a-vos-questions
https://www.gouvernement.fr/info-coronavirus/questions-reponses
Pour toute question contact@tousanticovid.gouv.fr ou le 0 800 087 148
juillet 2021
https://www.gouvernement.fr/pass-sanitaire-toutes-les-reponses-a-vos-questions
https://www.gouvernement.fr/info-coronavirus/questions-reponses
Pour toute question contact@tousanticovid.gouv.fr ou le 0 800 087 148
juillet 2021
BOURRAN – NOUVEAUX HORAIRES
NOUVEAUX HORAIRES A COMPTER du 27/09/2021
Site de BOURRAN
OUVERTURE du LABORATOIRE
Du LUNDI au VENDREDI de 7h30 à 12h30 et de 13h30 à 16h00
Le SAMEDI de 7h30 à 12h
«COMMENT SE PASSE UN PRÉLÈVEMENT NASOPHARYNGÉ ?», «LES TESTS PCR ET SEROLOGIQUES C’EST QUOI ?»
Toutes les informations dans cette vidéo …
mai 2020
Les calculs urinaires : éviter la récidive
Le calcul urinaire (lithiase) est une pathologie fréquente qui touche, selon les études, 4 à 20% de la population. La lithiase urinaire récidive dans 60% des cas et elle est multirécidivante chez 5 à 6% des patients, avec un risque d’évolution vers l’insuffisance rénale.
Son caractère récidivant et les complications que peuvent engendrer un calcul urinaire rendent nécessaire sa prévention et son traitement.
Les facteurs favorisants
-Facteurs alimentaires
Les risques sont accrus en fonction :
-des apports alimentaires : produits laitiers, protéines animales, sel, aliments riches en oxalate (chocolat, fruits secs, épinards, oseille, rhubarbe, thé), purines (abats, charcuterie,…), sucres rapides (fructose) ;
-de la diminution de la consommation de fibres alimentaires ;
-de l’excrétion urinaire insuffisante par insuffisance des apports de liquide.
-Facteurs familiaux
On retrouve une histoire familiale dans près de 40 % des cas
-Infections urinaires
Certains germes, comme Proteus et Klebsiella, favorisent les calculs phospho-ammoniaco-magnésiens.
-Anomalies du pH
Le pH normal des urines est de 5,8.
Un pH acide favorise la formation des calculs d’acide urique, de cystine et d’oxalate de calcium.
Un pH alcalin favorise la lithiase infectieuse et phospho-calcique.
Anomalies anatomiques
Certaines anomalies anatomiques des reins ou de la voie excrétrice empêchent l’écoulement normal des urines et donc favorise la formation des calculs.
Calculs médicamenteux
Les calculs médicamenteux sont peu fréquents puisqu’ils ne sont présents que dans 1 % des cas, mais on pense que leur fréquence est sous-estimée.
Maladies génétiques
Cystinose…
-Connaître la composition d’un calcul est essentiel : cela influence non seulement le traitement du calcul mais également le risque de récidive et la prise en charge à long terme.
Il est donc indispensable de recueillir les cristaux urinaires et des les faire analyser
Lors de la crise, on peut tamiser ces urines (à travers un filtre à café) ou recueillir le calcul dans une compresse.
Celui-ci sera alors déposé dans un flacon sans poudre et transmis au laboratoire (idéalement préalablement lavé et séché à température ambiante).
-Réaliser un bilan sanguin et urinaire de première intention
Ce bilan est actuellement systématiquement prescrit dès le premier épisode.
Il comprend :
-un bilan sanguin : créatininémie, calcémie, glycémie à jeun, uricémie ;
-un bilan sur urines de 24 h : créatinine, volume total (diurèse de 24h), calcium, sodium, urée, urates, citrates;
-un bilan sur urines du matin (à jeun) : pH, densité, cytologie, cristallurie.
Les conditions de recueil des urines vous seront précisées au laboratoire.
Il est important de ne pas modifier ses habitudes alimentaires pour la réalisation de ce bilan.
Il doit être réalisé à plus d’un mois d’un épisode aigu ou d’un geste urologique.
En conclusion :
mars 2020
Les facteurs favorisants
-Facteurs alimentaires
Les risques sont accrus en fonction :
-des apports alimentaires : produits laitiers, protéines animales, sel, aliments riches en oxalate (chocolat, fruits secs, épinards, oseille, rhubarbe, thé), purines (abats, charcuterie,…), sucres rapides (fructose) ;
-de la diminution de la consommation de fibres alimentaires ;
-de l’excrétion urinaire insuffisante par insuffisance des apports de liquide.
-Facteurs familiaux
On retrouve une histoire familiale dans près de 40 % des cas
-Infections urinaires
Certains germes, comme Proteus et Klebsiella, favorisent les calculs phospho-ammoniaco-magnésiens.
-Anomalies du pH
Le pH normal des urines est de 5,8.
Un pH acide favorise la formation des calculs d’acide urique, de cystine et d’oxalate de calcium.
Un pH alcalin favorise la lithiase infectieuse et phospho-calcique.
Anomalies anatomiques
Certaines anomalies anatomiques des reins ou de la voie excrétrice empêchent l’écoulement normal des urines et donc favorise la formation des calculs.
Calculs médicamenteux
Les calculs médicamenteux sont peu fréquents puisqu’ils ne sont présents que dans 1 % des cas, mais on pense que leur fréquence est sous-estimée.
Maladies génétiques
Cystinose…

Quel bilan pour éviter la récidive ?
-Connaître la composition d’un calcul est essentiel : cela influence non seulement le traitement du calcul mais également le risque de récidive et la prise en charge à long terme.
Il est donc indispensable de recueillir les cristaux urinaires et des les faire analyser
Lors de la crise, on peut tamiser ces urines (à travers un filtre à café) ou recueillir le calcul dans une compresse.
Celui-ci sera alors déposé dans un flacon sans poudre et transmis au laboratoire (idéalement préalablement lavé et séché à température ambiante).
-Réaliser un bilan sanguin et urinaire de première intention
Ce bilan est actuellement systématiquement prescrit dès le premier épisode.
Il comprend :
-un bilan sanguin : créatininémie, calcémie, glycémie à jeun, uricémie ;
-un bilan sur urines de 24 h : créatinine, volume total (diurèse de 24h), calcium, sodium, urée, urates, citrates;
-un bilan sur urines du matin (à jeun) : pH, densité, cytologie, cristallurie.
Les conditions de recueil des urines vous seront précisées au laboratoire.
Il est important de ne pas modifier ses habitudes alimentaires pour la réalisation de ce bilan.
Il doit être réalisé à plus d’un mois d’un épisode aigu ou d’un geste urologique.
En conclusion :
- La lithiase urinaire est une pathologie fréquente et récidivante, pouvant évoluer de longues années à bas bruit ou bien nécessiter un traitement en urgence et engager le pronostic vital.
- Le bilan au long cours de la lithiase urinaire repose sur un bilan sanguin et urinaire exhaustif et sur l’analyse du (des) calcul(s). Cela est essentiel pour le traitement mais également le risque de récidive et la prise en charge à long terme.
- Les règles hygiéno-diététiques, et principalement une diurèse de plus de 2 L/j, sont essentielles afin d’éviter la récidive lithiasique.
- La lithiase urinaire est une pathologie nécessitant une surveillance régulière et à vie.
mars 2020
La goutte et les analyses médicales
Ce qu’il est important de savoir :
Régime alimentaire
Différence entre la crise de la goute (accès aigu) et l’hyperuricémie
Traitement de la crise :
Traitement de l’hyperuricémie :
Suivi biologique de la maladie
source : http://www.rhumatologie.asso.fr/05-bibliotheque/publications/pub-74-160-167.asp
octobre 2019

Régime alimentaire
- Importance du régime et surtout de la réduction de consommation d’alcool, qui parfois peut permettre de traiter efficacement un malade apparemment « rebelle » à l’allopurinol…
- Arrêt définitif de la bière (même sans alcool)
Différence entre la crise de la goute (accès aigu) et l’hyperuricémie
- Différence entre accès aigu et hyperuricémie (taux d’acide urique dans le sang) qui ne sont pas liés
- Distinguo entre traitement de l’accès et traitement de la maladie métabolique
Traitement de la crise :
- Bon usage de la colchicine efficace lorsqu’elle est débutée le plus près possible du début de la crise
- Intérêt du glaçage articulaire
Traitement de l’hyperuricémie :
- Possibilité de crises en début de traitement par allopurinol : cela n’est pas un signe d’échec mais le signe de la bonne mobilisation des stocks d’urate
- Importance de la prévention des accès sous allopurinol — qui peuvent durer plusieurs mois, voire un an — grâce à la prescription systématique (et à la prise…) de colchicine (1 mg/j éventuellement en deux prises)
- Risque d’accès goutteux en cas d’arrêt de l’allopurinol
Suivi biologique de la maladie
- Utiliser le dosage de l’uricémie comme guide du traitement (au même titre que le dosage du cholestérol ou la pression artérielle)
- Objectif de l’allopurinol : abaisser l’uricémie en dessous de 360 μmol/l (60 mg/l)
- Vérification semestrielle puis annuelle de la stabilité de l’uricémie qui doit se maintenir en dessous de 360 μmol/l (60 mg/l), voire même en dessous chez certains malades atteints d’une goutte tophacée
- Surveillance annuelle de la fonction rénale (tolérance des AINS, de l’HTA, etc.)
source : http://www.rhumatologie.asso.fr/05-bibliotheque/publications/pub-74-160-167.asp
octobre 2019
Prévention du cancer de l’estomac
Une bactérie responsable : HELICOBACTER PYLORI
Avec 6556 nouveaux cas en 2012, le cancer de l’estomac est un des plus fréquents en France. La bactérie Helicobacter pylori est responsable d’au moins 80 % des cancers de l’estomac. Elle provoque chez la personne infectée une inflammation chronique de la muqueuse gastrique, c’est-à-dire une gastrite. L’acquisition d’H. pylori se fait pendant l’enfance et l’infection persiste toute la vie si elle n’est pas traitée. Le plus souvent, elle passe inaperçue mais peut provoquer des troubles digestifs ou évoluer vers une ulcère, c’est-à-dire une plaie de l’estomac plus étendue. Toutefois, 1 % des personnes infectées par la bactérie développent un cancer gastrique. Un traitement antibiotique en vue de l’éradication de la bactérie est donc nécessaire.
Quels sont les FACTEURS DE RISQUE du cancer de l’estomac ?
Un facteur de risque désigne un élément qui peut favoriser le développement d’une maladie. La présence d’un ou plusieurs facteurs de risque n’entraîne pas systématiquement l’apparition d’un cancer. Les principaux facteurs de risque reconnus du cancer de l’estomac sont :
Quels sont les MOYENS DE PREVENTION du cancer de l’estomac ?
ET ENSUITE ?
Si la présence de la bactérie est confirmée, le médecin proposera un traitement adapté pour l’éliminer, et ainsi éviter la survenue d’un ulcère et réduire le risque de développer un cancer de l’estomac. Il s’agit d’une association de plusieurs antibiotiques, à prendre pendant 10 ou 14j. Plus le traitement de l’infection a lieu tôt plus il est efficace pour prévenir l’apparition d’un cancer de l’estomac.
Au moins 4 semaines après la fin du traitement antibiotiques, un test respiratoire est systématiquement réalisé au laboratoire. Il permet de contrôler l’éradication de la bactérie et donc de s’assurer de l’efficacité du traitement.
Comment dois-je préparer le test respiratoire ?
Il doit être réalisé :
Information réalisée à partir du thésaurus dirigé par la société Nationale Française de Gastro-entérologie (juin 2019), des recommandations de diagnostic et de traitement de l’infection par H. pylori de l’HAS (mai 2017),
Pour aller plus loin, des brochures sont disponibles : InCa (2018) : https://www.e-cancer.fr/Comprendre-prevenir-depister/Reduire-les-risques-de-cancer/Infections/Infection-par-H.-pylori-et-cancer-de-l-estomac Brochure HAS (2019) : https://www.has-sante.fr/upload/docs/application/pdf/2019-03/helicobacter_recherche.pdf
mise à jour août 2019
Avec 6556 nouveaux cas en 2012, le cancer de l’estomac est un des plus fréquents en France. La bactérie Helicobacter pylori est responsable d’au moins 80 % des cancers de l’estomac. Elle provoque chez la personne infectée une inflammation chronique de la muqueuse gastrique, c’est-à-dire une gastrite. L’acquisition d’H. pylori se fait pendant l’enfance et l’infection persiste toute la vie si elle n’est pas traitée. Le plus souvent, elle passe inaperçue mais peut provoquer des troubles digestifs ou évoluer vers une ulcère, c’est-à-dire une plaie de l’estomac plus étendue. Toutefois, 1 % des personnes infectées par la bactérie développent un cancer gastrique. Un traitement antibiotique en vue de l’éradication de la bactérie est donc nécessaire.
Quels sont les FACTEURS DE RISQUE du cancer de l’estomac ?
Un facteur de risque désigne un élément qui peut favoriser le développement d’une maladie. La présence d’un ou plusieurs facteurs de risque n’entraîne pas systématiquement l’apparition d’un cancer. Les principaux facteurs de risque reconnus du cancer de l’estomac sont :
- une gastrite chronique causée par H.pylori,
- le tabagisme et la consommation d’alcool,
- une alimentation riche en produits salés et pauvre en légumes et en fruits frais,
- des antécédents familiaux de cancer de l’estomac (parents, frères, sœurs, enfants)
- une prédisposition génétique augmentant le risque de développer un cancer de l’estomac (syndrome de Lynch ou mutation du gène CDH1),
- avoir un ou plusieurs parents proches qui ont développé un cancer de l’estomac, en particulier à un âge jeune,
- la maladie de Biermer (gastrite entrainant une carence en vitamine B12 et un déficit en globules rouges),
- un antécédent de chirurgie gastrique (ce risque augmente à partir de 10-15 ans après l’intervention).
Quels sont les MOYENS DE PREVENTION du cancer de l’estomac ?

- Diagnostic des infections à H.pylori :
- Dépistage de l’entourage d’un patient suivi pour un cancer de l’estomac :
- un test respiratoire ou une sérologie, réalisables en laboratoire de biologie médicale, pour les patients de moins de 45 ans.
- une fibroscopie digestive, pour les patients de plus de 45 ans.
- Autres situations :
ET ENSUITE ?
Si la présence de la bactérie est confirmée, le médecin proposera un traitement adapté pour l’éliminer, et ainsi éviter la survenue d’un ulcère et réduire le risque de développer un cancer de l’estomac. Il s’agit d’une association de plusieurs antibiotiques, à prendre pendant 10 ou 14j. Plus le traitement de l’infection a lieu tôt plus il est efficace pour prévenir l’apparition d’un cancer de l’estomac.
Au moins 4 semaines après la fin du traitement antibiotiques, un test respiratoire est systématiquement réalisé au laboratoire. Il permet de contrôler l’éradication de la bactérie et donc de s’assurer de l’efficacité du traitement.
Comment dois-je préparer le test respiratoire ?
Il doit être réalisé :
- au moins 4 semaines après l’arrêt des antibiotiques
- et au moins 2 semaines après l’arrêt des IPP
- au moins 24h après l’arrêt des antiacides et des pansements gastro-intestinaux
Information réalisée à partir du thésaurus dirigé par la société Nationale Française de Gastro-entérologie (juin 2019), des recommandations de diagnostic et de traitement de l’infection par H. pylori de l’HAS (mai 2017),
Pour aller plus loin, des brochures sont disponibles : InCa (2018) : https://www.e-cancer.fr/Comprendre-prevenir-depister/Reduire-les-risques-de-cancer/Infections/Infection-par-H.-pylori-et-cancer-de-l-estomac Brochure HAS (2019) : https://www.has-sante.fr/upload/docs/application/pdf/2019-03/helicobacter_recherche.pdf
mise à jour août 2019
Le bon usage des antibiotiques par les patients
L’usage abusif et trop souvent incorrect des antibiotiques a contribué à l’apparition et à la dissémination de bactéries qui sont devenues résistantes aux antibiotiques. Ce phénomène est devenu progressivement un problème majeur de santé publique pour la France et dans le monde entier.
Qu’est-ce qu’un ANTIBIOTIQUE ?
En 1928, la découverte de l’action « antibiotique » d’un champignon appelé le Penicillium, a donné naissance au premier antibiotique, « la pénicilline ». Celui-ci a révolutionné la médecine en diminuant très largement le nombre de décès par infections bactériennes très courantes à l’époque pré-antibiotique. Aujourd’hui, il existe plusieurs classes d’antibiotiques, ce sont des médicaments d’origine naturelle, semi-synthétiques ou de synthèse.
LES ANTIBIOTIQUES, à quoi servent-ils ?
 Depuis des décennies, les antibiotiques ont permis de soigner des infections bactériennes et de réduire considérablement la mortalité par maladies infectieuses, comme la pneumonie ou la tuberculose. Première cause de mortalité en 1940, ces maladies ne sont aujourd’hui responsables que de 2 % des décès en France. Les antibiotiques sont efficaces uniquement contre les bactéries.
Depuis des décennies, les antibiotiques ont permis de soigner des infections bactériennes et de réduire considérablement la mortalité par maladies infectieuses, comme la pneumonie ou la tuberculose. Première cause de mortalité en 1940, ces maladies ne sont aujourd’hui responsables que de 2 % des décès en France. Les antibiotiques sont efficaces uniquement contre les bactéries.
Les infections virales (rhino-pharyngite, bronchite aiguë, grippe, rhume…) et les infections bactériennes (tuberculose, cystite, pneumonie…) présentent des symptômes souvent similaires (fièvre, toux, troubles digestifs, courbatures) mais elles ne doivent pas être traitées de la même manière. Par exemple, 75 à 90 % des cas d’angine chez l’adulte ou 60 à 75 % chez l’enfant sont d’origine virale et dans ces cas-là, les antibiotiques ne sont pas efficaces car ils n’agissent pas sur les virus. Ils ne permettent pas au patient de guérir plus vite ni de se protéger des infections virales transmises par d’autres personnes. En cas de maladies virales courantes, la guérison survient naturellement en 1 à 2 semaines, sans antibiotiques. En cas de persistance ou d’aggravation des symptômes, il est toutefois nécessaire de consulter à nouveau son médecin.
Seul un médecin fera le bon diagnostic et pourra décider si le patient a effectivement besoin d’un traitement antibiotique.
L’ANTIBIORESISTANCE, qu’est-ce que c’est ?
Pour une bactérie, l’antibiorésistance est la capacité, à devenir résistante aux antibiotiques, en développant des mécanismes de défense, diminuant ou annulant l’action des antibiotiques qui la combattent. Ce phénomène touche aussi bien les bactéries à l’origine des infections que les bactéries généralement inoffensives qui sont naturellement présentes sur notre corps, chez les animaux (de compagnie ou de production alimentaire) et dans l’environnement. Lorsque la résistance s’est développée chez l’une ou l’autre de ces espèces bactériennes, elle peut être transmise à d’autres espèces, et ainsi contribuer à l’expansion du phénomène et à sa diffusion. Les antibiotiques deviennent ainsi inefficaces et ne peuvent plus nous soigner contre des infections à bactéries résistantes.
Les antibiotiques peuvent-ils soigner des INFECTIONS PRODUITES PAR DES BACTERIES RESISTANTES ?
Les antibiotiques prescrits habituellement par le médecin (dits « de première ligne ») peuvent ne pas être efficaces contre des infections provoquées par des bactéries résistantes, il faut alors avoir recours à des antibiotiques plus puissants. Cependant, il peut arriver que des antibiotiques efficaces viennent à manquer pour traiter certaines infections, aboutissant à des situations où il n’existe plus aucun traitement possible ; on parle alors « d’impasse thérapeutique ». Cette difficulté est accentuée par l’absence de développement d’antibiotiques possédant un nouveau mécanisme d’action, au cours des 20 dernières années.
L’ANTIBIORESISTANCE, quelle en est la cause ?
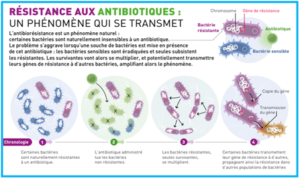 Depuis la découverte de la pénicilline, chaque nouvelle génération d’antibiotiques a vu apparaître des mécanismes de résistance lui correspondant. Une bactérie peut échapper à l’action d’un antibiotique, du fait d’une mutation génétique, ou par acquisition d’un gène de résistance transmis par une autre bactérie, souvent favorisés par l’exposition aux antibiotiques. En se multipliant, la bactérie va transmettre sa résistance aux antibiotiques à sa descendance. Plus on prend d’antibiotiques, plus le risque s’accroît de faire émerger des bactéries résistantes qui rendent les traitements antibiotiques ultérieurs moins efficaces. Aujourd’hui, de nouvelles résistances bactériennes se multiplient, en ville, comme à l’hôpital, et poussent les médecins à utiliser des antibiotiques toujours plus puissants. L’usage répété de ceux-ci contribue aussi à renforcer l’émergence de résistances à ces antibiotiques plus puissants.
Depuis la découverte de la pénicilline, chaque nouvelle génération d’antibiotiques a vu apparaître des mécanismes de résistance lui correspondant. Une bactérie peut échapper à l’action d’un antibiotique, du fait d’une mutation génétique, ou par acquisition d’un gène de résistance transmis par une autre bactérie, souvent favorisés par l’exposition aux antibiotiques. En se multipliant, la bactérie va transmettre sa résistance aux antibiotiques à sa descendance. Plus on prend d’antibiotiques, plus le risque s’accroît de faire émerger des bactéries résistantes qui rendent les traitements antibiotiques ultérieurs moins efficaces. Aujourd’hui, de nouvelles résistances bactériennes se multiplient, en ville, comme à l’hôpital, et poussent les médecins à utiliser des antibiotiques toujours plus puissants. L’usage répété de ceux-ci contribue aussi à renforcer l’émergence de résistances à ces antibiotiques plus puissants.
L’ANTIBIORESISTANCE, quelles conséquences ?
L’antibiorésistance est un grave problème de santé publique mondial, qui progresse extrêmement rapidement, et qui s’accélère depuis les années 2000. Elle menace notre mode de vie actuel et compromet toutes les avancées que la médecine a effectuées depuis plus de 70 ans. Si les habitudes de surconsommation d’antibiotiques ne sont pas stoppées, l’antibiorésistance pourrait devenir l’une des principales causes de mortalité dans le monde. Il a été évalué qu’en 2050, les maladies infectieuses d’origine bactériennes pourraient en effet provoquer jusqu’à 10 millions de morts par an, soit plus de le cancer. Le rapport de l’Organisation mondiale de la santé de 2014, parle même d’une future ère postantibiotiques, « où des infections courantes et des blessures mineures qui ont été soignées depuis des décennies pourraient à nouveau tuer ».
Les infections bactériennes seraient plus longues et plus difficiles à soigner ; nécessitant l’emploi d’antibiotiques plus puissants et plus chers et le risque de décès causés par des infections bactériennes jusqu’alors faciles à traiter serait beaucoup plus important. De plus, depuis la découverte de la pénicilline, la médecine a fait des progrès considérables en matière de chirurgie complexe, de greffes d’organes, de néonatalogie ou de réanimation. Toutes ces interventions deviendraient impossibles si l’antibiorésistance se développait davantage, car le risque infectieux provoqué par chaque geste médical serait trop élevé.
Comment LIMITER L’ANTIBIORESISTANCE ?
Pour limiter le développement de ces bactéries résistantes, chacun peu adopter un bon usage des antibiotiques et une attitude responsable pour limiter la survenues d’infections, selon les recommandations nationales de l’Agence nationale de sécurité du médicament (ANSM) et du Ministère des Solidarité et de la Santé :
Adopter un « bon usage » des antibiotiques
– Ne pas prendre d’antibiotiques sans prescription d’un médecin ;
– Respecter la prescription du médecin (dose, fréquence, durée) et ne pas arrêter un traitement prématurément, même si l’état s’améliore.
– Ne pas prendre d’antibiotiques utilisés ou non utilisés lors d’un précédent traitement même si les symptômes semblent les mêmes ; et ne pas donner son traitement à quelqu’un d’autre (un antibiotique est spécifique à chaque personne) ;
– Signaler tout effet indésirable survenu pendant le traitement à son pharmacien ou à son médecin ;
– A la fin du traitement, rapporter à son pharmacien toutes les boîtes d’antibiotiques entamées ou non pour destruction et ne pas les jeter dans les toilettes, la poubelle ou l’environnement.
Prévenir les infections

– Hygiène des mains : surtout dans les moments suivants : passage aux toilettes, retour à son domicile, avant de préparer un repas, après avoir éternué / s’être mouché, avant et après avoir pris soin d’une personne.
– Hygiène alimentaire : conserver les aliments et préparer les repas dans des conditions adaptées à chaque aliment.
– Vaccination : contre les infections bactériennes, elle est un moyen d’éviter la maladie, donc le traitement antibiotique éventuel, qui pourrait se révéler inefficace du fait d’une antibiorésistance. Elle permet également d’éviter l’effet indésirable des antibiotiques sur notre flore intestinale.
Information réalisée à partir des plaquettes des recommandations associées de l’ANSM, Santé publique France, ANSES, de l’Assurances maladie et de l’INSERM (plaquettes de novembre 2018 et novembre 2017) (09/2017), du dossier d’information du Ministère des Solidarité et de la Santé (juin 2018) et de l’institut Pasteur (mars 2017). Pour en savoir plus, des dépliants sont disponibles sur les sites internet de : – L’Assurance maladie : https://www.ameli.fr/ Brochure « Les antibiotiques, utilisés à tort, ils deviendront moins forts » (2011) et dossier « Bien utiliser les antibiotiques » (2018) – Ministère des solidarités et de la santé : https://solidarites-sante.gouv.fr Dossier : les antibiotiques sauvent des vies (2018) – ANSM : https://www.ansm.sante.fr Dépliants « Une infection évitée c’est un antibiotique préservé » (2018) et « Consommation d’antibiotiques et résistance aux antibiotiques en France : soyons concernés, soyons responsables (2019) – CPIAS : http://www.cpias.fr/campagnes/antibiotiques/bon-usage-antibiotiques.htm Dépliant « Les antibios c’est juste quand il faut ! » et « La résistance des bactéries aux antibiotiques »
mise à jour août 2019
Qu’est-ce qu’un ANTIBIOTIQUE ?
En 1928, la découverte de l’action « antibiotique » d’un champignon appelé le Penicillium, a donné naissance au premier antibiotique, « la pénicilline ». Celui-ci a révolutionné la médecine en diminuant très largement le nombre de décès par infections bactériennes très courantes à l’époque pré-antibiotique. Aujourd’hui, il existe plusieurs classes d’antibiotiques, ce sont des médicaments d’origine naturelle, semi-synthétiques ou de synthèse.
LES ANTIBIOTIQUES, à quoi servent-ils ?
 Depuis des décennies, les antibiotiques ont permis de soigner des infections bactériennes et de réduire considérablement la mortalité par maladies infectieuses, comme la pneumonie ou la tuberculose. Première cause de mortalité en 1940, ces maladies ne sont aujourd’hui responsables que de 2 % des décès en France. Les antibiotiques sont efficaces uniquement contre les bactéries.
Depuis des décennies, les antibiotiques ont permis de soigner des infections bactériennes et de réduire considérablement la mortalité par maladies infectieuses, comme la pneumonie ou la tuberculose. Première cause de mortalité en 1940, ces maladies ne sont aujourd’hui responsables que de 2 % des décès en France. Les antibiotiques sont efficaces uniquement contre les bactéries.
Les infections virales (rhino-pharyngite, bronchite aiguë, grippe, rhume…) et les infections bactériennes (tuberculose, cystite, pneumonie…) présentent des symptômes souvent similaires (fièvre, toux, troubles digestifs, courbatures) mais elles ne doivent pas être traitées de la même manière. Par exemple, 75 à 90 % des cas d’angine chez l’adulte ou 60 à 75 % chez l’enfant sont d’origine virale et dans ces cas-là, les antibiotiques ne sont pas efficaces car ils n’agissent pas sur les virus. Ils ne permettent pas au patient de guérir plus vite ni de se protéger des infections virales transmises par d’autres personnes. En cas de maladies virales courantes, la guérison survient naturellement en 1 à 2 semaines, sans antibiotiques. En cas de persistance ou d’aggravation des symptômes, il est toutefois nécessaire de consulter à nouveau son médecin.
Seul un médecin fera le bon diagnostic et pourra décider si le patient a effectivement besoin d’un traitement antibiotique.
L’ANTIBIORESISTANCE, qu’est-ce que c’est ?
Pour une bactérie, l’antibiorésistance est la capacité, à devenir résistante aux antibiotiques, en développant des mécanismes de défense, diminuant ou annulant l’action des antibiotiques qui la combattent. Ce phénomène touche aussi bien les bactéries à l’origine des infections que les bactéries généralement inoffensives qui sont naturellement présentes sur notre corps, chez les animaux (de compagnie ou de production alimentaire) et dans l’environnement. Lorsque la résistance s’est développée chez l’une ou l’autre de ces espèces bactériennes, elle peut être transmise à d’autres espèces, et ainsi contribuer à l’expansion du phénomène et à sa diffusion. Les antibiotiques deviennent ainsi inefficaces et ne peuvent plus nous soigner contre des infections à bactéries résistantes.
Les antibiotiques peuvent-ils soigner des INFECTIONS PRODUITES PAR DES BACTERIES RESISTANTES ?
Les antibiotiques prescrits habituellement par le médecin (dits « de première ligne ») peuvent ne pas être efficaces contre des infections provoquées par des bactéries résistantes, il faut alors avoir recours à des antibiotiques plus puissants. Cependant, il peut arriver que des antibiotiques efficaces viennent à manquer pour traiter certaines infections, aboutissant à des situations où il n’existe plus aucun traitement possible ; on parle alors « d’impasse thérapeutique ». Cette difficulté est accentuée par l’absence de développement d’antibiotiques possédant un nouveau mécanisme d’action, au cours des 20 dernières années.
L’ANTIBIORESISTANCE, quelle en est la cause ?
 Depuis la découverte de la pénicilline, chaque nouvelle génération d’antibiotiques a vu apparaître des mécanismes de résistance lui correspondant. Une bactérie peut échapper à l’action d’un antibiotique, du fait d’une mutation génétique, ou par acquisition d’un gène de résistance transmis par une autre bactérie, souvent favorisés par l’exposition aux antibiotiques. En se multipliant, la bactérie va transmettre sa résistance aux antibiotiques à sa descendance. Plus on prend d’antibiotiques, plus le risque s’accroît de faire émerger des bactéries résistantes qui rendent les traitements antibiotiques ultérieurs moins efficaces. Aujourd’hui, de nouvelles résistances bactériennes se multiplient, en ville, comme à l’hôpital, et poussent les médecins à utiliser des antibiotiques toujours plus puissants. L’usage répété de ceux-ci contribue aussi à renforcer l’émergence de résistances à ces antibiotiques plus puissants.
Depuis la découverte de la pénicilline, chaque nouvelle génération d’antibiotiques a vu apparaître des mécanismes de résistance lui correspondant. Une bactérie peut échapper à l’action d’un antibiotique, du fait d’une mutation génétique, ou par acquisition d’un gène de résistance transmis par une autre bactérie, souvent favorisés par l’exposition aux antibiotiques. En se multipliant, la bactérie va transmettre sa résistance aux antibiotiques à sa descendance. Plus on prend d’antibiotiques, plus le risque s’accroît de faire émerger des bactéries résistantes qui rendent les traitements antibiotiques ultérieurs moins efficaces. Aujourd’hui, de nouvelles résistances bactériennes se multiplient, en ville, comme à l’hôpital, et poussent les médecins à utiliser des antibiotiques toujours plus puissants. L’usage répété de ceux-ci contribue aussi à renforcer l’émergence de résistances à ces antibiotiques plus puissants.
L’ANTIBIORESISTANCE, quelles conséquences ?
L’antibiorésistance est un grave problème de santé publique mondial, qui progresse extrêmement rapidement, et qui s’accélère depuis les années 2000. Elle menace notre mode de vie actuel et compromet toutes les avancées que la médecine a effectuées depuis plus de 70 ans. Si les habitudes de surconsommation d’antibiotiques ne sont pas stoppées, l’antibiorésistance pourrait devenir l’une des principales causes de mortalité dans le monde. Il a été évalué qu’en 2050, les maladies infectieuses d’origine bactériennes pourraient en effet provoquer jusqu’à 10 millions de morts par an, soit plus de le cancer. Le rapport de l’Organisation mondiale de la santé de 2014, parle même d’une future ère postantibiotiques, « où des infections courantes et des blessures mineures qui ont été soignées depuis des décennies pourraient à nouveau tuer ».
Les infections bactériennes seraient plus longues et plus difficiles à soigner ; nécessitant l’emploi d’antibiotiques plus puissants et plus chers et le risque de décès causés par des infections bactériennes jusqu’alors faciles à traiter serait beaucoup plus important. De plus, depuis la découverte de la pénicilline, la médecine a fait des progrès considérables en matière de chirurgie complexe, de greffes d’organes, de néonatalogie ou de réanimation. Toutes ces interventions deviendraient impossibles si l’antibiorésistance se développait davantage, car le risque infectieux provoqué par chaque geste médical serait trop élevé.
Comment LIMITER L’ANTIBIORESISTANCE ?

Pour limiter le développement de ces bactéries résistantes, chacun peu adopter un bon usage des antibiotiques et une attitude responsable pour limiter la survenues d’infections, selon les recommandations nationales de l’Agence nationale de sécurité du médicament (ANSM) et du Ministère des Solidarité et de la Santé :
– Ne pas prendre d’antibiotiques sans prescription d’un médecin ;
– Respecter la prescription du médecin (dose, fréquence, durée) et ne pas arrêter un traitement prématurément, même si l’état s’améliore.
– Ne pas prendre d’antibiotiques utilisés ou non utilisés lors d’un précédent traitement même si les symptômes semblent les mêmes ; et ne pas donner son traitement à quelqu’un d’autre (un antibiotique est spécifique à chaque personne) ;
– Signaler tout effet indésirable survenu pendant le traitement à son pharmacien ou à son médecin ;
– A la fin du traitement, rapporter à son pharmacien toutes les boîtes d’antibiotiques entamées ou non pour destruction et ne pas les jeter dans les toilettes, la poubelle ou l’environnement.

– Hygiène des mains : surtout dans les moments suivants : passage aux toilettes, retour à son domicile, avant de préparer un repas, après avoir éternué / s’être mouché, avant et après avoir pris soin d’une personne.
– Hygiène alimentaire : conserver les aliments et préparer les repas dans des conditions adaptées à chaque aliment.
– Vaccination : contre les infections bactériennes, elle est un moyen d’éviter la maladie, donc le traitement antibiotique éventuel, qui pourrait se révéler inefficace du fait d’une antibiorésistance. Elle permet également d’éviter l’effet indésirable des antibiotiques sur notre flore intestinale.
Information réalisée à partir des plaquettes des recommandations associées de l’ANSM, Santé publique France, ANSES, de l’Assurances maladie et de l’INSERM (plaquettes de novembre 2018 et novembre 2017) (09/2017), du dossier d’information du Ministère des Solidarité et de la Santé (juin 2018) et de l’institut Pasteur (mars 2017). Pour en savoir plus, des dépliants sont disponibles sur les sites internet de : – L’Assurance maladie : https://www.ameli.fr/ Brochure « Les antibiotiques, utilisés à tort, ils deviendront moins forts » (2011) et dossier « Bien utiliser les antibiotiques » (2018) – Ministère des solidarités et de la santé : https://solidarites-sante.gouv.fr Dossier : les antibiotiques sauvent des vies (2018) – ANSM : https://www.ansm.sante.fr Dépliants « Une infection évitée c’est un antibiotique préservé » (2018) et « Consommation d’antibiotiques et résistance aux antibiotiques en France : soyons concernés, soyons responsables (2019) – CPIAS : http://www.cpias.fr/campagnes/antibiotiques/bon-usage-antibiotiques.htm Dépliant « Les antibios c’est juste quand il faut ! » et « La résistance des bactéries aux antibiotiques »
mise à jour août 2019
Comment traiter la gale efficacement ?
QU’EST-CE QUE LA GALE ?
La gale humaine est une maladie de la peau due à un sarcopte, minuscule parasite de la famille des acariens qui a la capacité de pénétrer l’épiderme et de s’y reproduire. C’est une maladie contagieuse, pouvant toucher tous types de personnes, quels que soient leur âge, leur hygiène et leur milieu social. Elle s’attrape par contact direct et prolongé de la peau avec une personne porteuse de la gale ou par contact des vêtements, du linge de maison, de la literie contaminées.
Il n’existe pas de surveillance spécifique de la gale. Mais les différentes études disponibles montrent une recrudescence de la gale. Elle sévit par « petites épidémies » dans les collectivités : maisons de retraite, services hospitaliers, écoles… Des épisodes de gale sont régulièrement signalés.
Quels sont les SYMPTOMES DE LA GALE ?
Les symptômes de la gale surviennent après une période d’incubation de trois semaines en moyenne. Les principaux symptômes révélateurs de la gale sont des démangeaisons et des lésions cutanées dus à une réaction allergique au sarcopte et à ses déjections. Les démangeaisons de la gale sont souvent plus prononcées la nuit. Ce prurit intense provoque des lésions de la peau appelées lésions de grattage pouvant ressembler à des lésions d’eczéma (rougeurs, croûtes). Elles sont localisées sur les zones du corps atteintes par le parasite de la gale : entre les doigts des mains ; à l’avant des poignets ; sur les coudes et les avant-bras ; au niveau du nombril ; à l’intérieur des cuisses ; au niveau des organes génitaux chez l’homme et des mamelons chez la femme ; sur les fesses. Dans la gale commune, le dos, le cou et le visage sont épargnés, sauf chez le nourrisson. En cas de gale profuse ou hyperkératosique, les lésions s’étendent à l’ensemble du corps, y compris au dos.
Quels est le TRAITEMENT DE LA GALE ?
Lorsque le diagnostic de gale est confirmé, le médecin prescrit un traitement. En effet, la maladie ne peut pas guérir d’elle-même. De plus, la gale étant très contagieuse, l’entourage doit être traité en même temps que la personne atteinte de la gale. Les soins doivent aussi s’accompagner d’un traitement du linge qui a pu être contaminé par le parasite (vêtements, sous-vêtements, draps et couvertures, serviettes de toilette, etc.). Deux types de traitement sont possibles, selon les cas :
Le traitement local
Il consiste à appliquer un produit scabicide (lotion, crème ou spray), sur tout le corps, y compris sur le cuir chevelu à l’exception du visage. Lors de l’application, insistez bien sur les zones où le sarcopte est le plus souvent présent. Ce produit est efficace à tous les stades du cycle de vie du parasite mais il peut provoquer des irritations. Commencez votre traitement de la gale un soir, en respectant les étapes suivantes : Prenez un bain et séchez-vous soigneusement ; changez vos draps et avant de vous coucher, appliquez sur la peau le produit prescrit, en suivant bien les recommandations de votre pharmacien et celles de la notice (zones du corps à protéger ou sur lesquelles insister) ; laissez agir le médicament pendant tout le temps prescrit, puis, lavez-vous pour éliminer les résidus de produit et changez de nouveau vos draps.
Le traitement par voie orale
Il se prend en une seule fois, sous la forme de comprimés. Plus simple et plus rapide que le traitement local, il est souvent prescrit lorsqu’il y a un nombre important de personnes à traiter (ex. : collectivités). Une deuxième prise 14 jours après la première est nécessaire car le médicament est inefficace sur les œufs du parasite de la gale.
Les deux traitements peuvent être parfois associés selon l’importance de l’infestation. D’autres médicaments peuvent aussi vous être prescrits si la gale entraîne des complications : un antibiotique en cas de surinfection bactérienne (impétigo) ; ou un antihistaminique en cas de démangeaisons importantes et persistantes. Si les démangeaisons persistent pendant 10 à 15 jours après le début du traitement de la gale, ne vous inquiétez pas. Au-delà de ce délai, consultez votre médecin.
LES MESURES INDISPENSABLES POUR ÉVITER LA TRANSMISSION DE LA GALE
La gale est une maladie très contagieuse. Pour éviter la transmission du sarcopte à ses proches et la propagation de la gale, il est important de bien suivre le traitement prescrit par le médecin traitant ainsi que les recommandations d’hygiène concernant la literie et les vêtements. Voici quelques conseils importants :
Informez le personnel des collectivités que vous fréquentez et toutes les personnes avec lesquelles vous avez été en contact prolongé et répété.
Evitez tout contact cutané avec votre entourage durant les 3 jours suivant la première prise de médicaments et abstenez-vous de relations sexuelles pendant tout le traitement ;
Se laver régulièrement les mains avec du savon, le gel hydroalcoolique étant inefficace ;
En cas de gale commune, passez l’aspirateur dans toute la maison et jetez immédiatement les sacs à aspirateur utilisés;
Si votre enfant est atteint de gale, il ne pourra retourner en collectivité (école, crèche, centre aéré) que 3 jours après le début du traitement. En attendant, gardez-le à votre domicile.
Gale : des consignes de lavage spécifiques pour le linge
– Il faut laver ce linge à la machine à 60 °C et le sécher à haute température si possible.
– Les tissus qui ne peuvent être lavés à l’eau chaude doivent être traités par contact avec une poudre ascaricide (qui tue les acariens), pendant au moins 48 heures. On peut aussi les entreposer pendant 1 semaine dans un sac en plastique étanche à l’air. En effet, le sarcopte ne survit pas plus de quatre jours en l’absence de contact avec la peau.
Information réalisée à partir des recommandations de l’assurance maladie (juin 2018), de l’ARS Occitanie (2014) et du Haut Conseil de la Santé Publique (2012). Deux dépliants sont disponibles sur : le site de l’ARS Occitanie et sur le site de la CPIAS nouvelle aquitaine : https://www.cpias-nouvelle-aquitaine.fr/wp-content/uploads/2015/11/Plaquette_2015_gale_usagers.pdf
mise à jour août 2019
La gale humaine est une maladie de la peau due à un sarcopte, minuscule parasite de la famille des acariens qui a la capacité de pénétrer l’épiderme et de s’y reproduire. C’est une maladie contagieuse, pouvant toucher tous types de personnes, quels que soient leur âge, leur hygiène et leur milieu social. Elle s’attrape par contact direct et prolongé de la peau avec une personne porteuse de la gale ou par contact des vêtements, du linge de maison, de la literie contaminées.
Il n’existe pas de surveillance spécifique de la gale. Mais les différentes études disponibles montrent une recrudescence de la gale. Elle sévit par « petites épidémies » dans les collectivités : maisons de retraite, services hospitaliers, écoles… Des épisodes de gale sont régulièrement signalés.
Quels sont les SYMPTOMES DE LA GALE ?

Les symptômes de la gale surviennent après une période d’incubation de trois semaines en moyenne. Les principaux symptômes révélateurs de la gale sont des démangeaisons et des lésions cutanées dus à une réaction allergique au sarcopte et à ses déjections. Les démangeaisons de la gale sont souvent plus prononcées la nuit. Ce prurit intense provoque des lésions de la peau appelées lésions de grattage pouvant ressembler à des lésions d’eczéma (rougeurs, croûtes). Elles sont localisées sur les zones du corps atteintes par le parasite de la gale : entre les doigts des mains ; à l’avant des poignets ; sur les coudes et les avant-bras ; au niveau du nombril ; à l’intérieur des cuisses ; au niveau des organes génitaux chez l’homme et des mamelons chez la femme ; sur les fesses. Dans la gale commune, le dos, le cou et le visage sont épargnés, sauf chez le nourrisson. En cas de gale profuse ou hyperkératosique, les lésions s’étendent à l’ensemble du corps, y compris au dos.
Quels est le TRAITEMENT DE LA GALE ?
Lorsque le diagnostic de gale est confirmé, le médecin prescrit un traitement. En effet, la maladie ne peut pas guérir d’elle-même. De plus, la gale étant très contagieuse, l’entourage doit être traité en même temps que la personne atteinte de la gale. Les soins doivent aussi s’accompagner d’un traitement du linge qui a pu être contaminé par le parasite (vêtements, sous-vêtements, draps et couvertures, serviettes de toilette, etc.). Deux types de traitement sont possibles, selon les cas :
Il consiste à appliquer un produit scabicide (lotion, crème ou spray), sur tout le corps, y compris sur le cuir chevelu à l’exception du visage. Lors de l’application, insistez bien sur les zones où le sarcopte est le plus souvent présent. Ce produit est efficace à tous les stades du cycle de vie du parasite mais il peut provoquer des irritations. Commencez votre traitement de la gale un soir, en respectant les étapes suivantes : Prenez un bain et séchez-vous soigneusement ; changez vos draps et avant de vous coucher, appliquez sur la peau le produit prescrit, en suivant bien les recommandations de votre pharmacien et celles de la notice (zones du corps à protéger ou sur lesquelles insister) ; laissez agir le médicament pendant tout le temps prescrit, puis, lavez-vous pour éliminer les résidus de produit et changez de nouveau vos draps.
Il se prend en une seule fois, sous la forme de comprimés. Plus simple et plus rapide que le traitement local, il est souvent prescrit lorsqu’il y a un nombre important de personnes à traiter (ex. : collectivités). Une deuxième prise 14 jours après la première est nécessaire car le médicament est inefficace sur les œufs du parasite de la gale.
Les deux traitements peuvent être parfois associés selon l’importance de l’infestation. D’autres médicaments peuvent aussi vous être prescrits si la gale entraîne des complications : un antibiotique en cas de surinfection bactérienne (impétigo) ; ou un antihistaminique en cas de démangeaisons importantes et persistantes. Si les démangeaisons persistent pendant 10 à 15 jours après le début du traitement de la gale, ne vous inquiétez pas. Au-delà de ce délai, consultez votre médecin.
LES MESURES INDISPENSABLES POUR ÉVITER LA TRANSMISSION DE LA GALE
La gale est une maladie très contagieuse. Pour éviter la transmission du sarcopte à ses proches et la propagation de la gale, il est important de bien suivre le traitement prescrit par le médecin traitant ainsi que les recommandations d’hygiène concernant la literie et les vêtements. Voici quelques conseils importants :
– Il faut laver ce linge à la machine à 60 °C et le sécher à haute température si possible.
– Les tissus qui ne peuvent être lavés à l’eau chaude doivent être traités par contact avec une poudre ascaricide (qui tue les acariens), pendant au moins 48 heures. On peut aussi les entreposer pendant 1 semaine dans un sac en plastique étanche à l’air. En effet, le sarcopte ne survit pas plus de quatre jours en l’absence de contact avec la peau.
Information réalisée à partir des recommandations de l’assurance maladie (juin 2018), de l’ARS Occitanie (2014) et du Haut Conseil de la Santé Publique (2012). Deux dépliants sont disponibles sur : le site de l’ARS Occitanie et sur le site de la CPIAS nouvelle aquitaine : https://www.cpias-nouvelle-aquitaine.fr/wp-content/uploads/2015/11/Plaquette_2015_gale_usagers.pdf
mise à jour août 2019